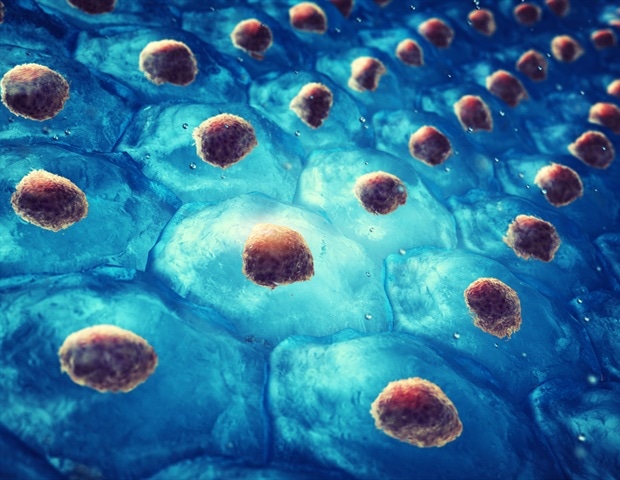
Используя новую модель на основе стволовых клеток, созданную из клеток кожи, ученые обнаружили первое прямое доказательство того, что мутации гена ABCA4 , связанные со Старгардтом , влияют на слой клеток в глазу, называемый пигментным эпителием сетчатки (ПЭС). Открытие указывает на новое понимание прогрессирования болезни Штаргардта и предлагает терапевтическую стратегию для болезни, которая в настоящее время не лечится. Исследование проводилось в Национальном глазном институте (NEI), входящем в состав Национального института здоровья. Результаты опубликованы сегодня в Интернете в отчетах о стволовых клетках.
Эта новая модель ускорит разработку методов лечения болезни Штаргардта. Нам не хватает терапии для этой болезни отчасти потому, что она встречается редко. Эта модель теоретически создает неограниченный запас человеческих клеток для изучения».
Майкл Ф. Чианг, доктор медицинских наук, директор NEI
Старгардт поражает примерно 1 из каждых 10 000 человек в США.
Болезнь Штаргардта вызывает прогрессирующую потерю центрального и ночного зрения. Потеря зрения связана с токсическим накоплением богатых липидами отложений в ПЭС, основная задача которых состоит в том, чтобы поддерживать и питать светочувствительные фоторецепторы сетчатки. В нормальных условиях ген ABCA4 вырабатывает белок, который предотвращает накопление токсинов. Предыдущие исследования показали, что болезнь Штаргардта вызывается различными мутациями в гене ABCA4 . Известно, что более 800 мутаций ABCA4 связаны с широким спектром фенотипов болезни Штаргардта.
Одним из способов, которым RPE поддерживает фоторецепторы, является проглатывание их отработанных внешних сегментов, что сохраняет клетку здоровой и здоровой. Многие ученые считают, что при болезни Штаргардта клетки ПЭС умирают после того, как приобретают токсичные побочные продукты при проглатывании наружных сегментов, что, в свою очередь, приводит к гибели фоторецепторов и потере зрения.
Большая часть современного понимания болезни Штаргардта была получена путем изучения моделей мышей, которые по своей природе ограничены из-за широкой генетической изменчивости болезни у людей. На человеческой модели RPE исследователи NEI смогли определить , влияют ли мутации гена ABCA4 на RPE напрямую, независимо от фоторецепторов.

Life Extension, MacuGuard, препарат с шафраном для укрепления зрения, 60 мягких таблеток
Чтобы разработать модель, исследователи взяли клетки кожи пациентов Старгардта, преобразовали их в стволовые клетки, а затем заставили стволовые клетки дифференцироваться в клетки ПЭС. Изучая RPE, полученный от пациента, исследователи обнаружили белок ABCA4 на клеточной мембране RPE. Они исследовали функцию ABCA4 в развитии RPE, используя технологию редактирования генов CRISPR/Cas9 для создания RPE, полученного от пациента, без ABCA4, называемого нокаутом ABCA4. Они обнаружили, что потеря ABCA4 не влияла на созревание RPE, полученного от пациента.
Однако, когда RPE, лишенный ABCA4, подвергался воздействию нормальных (дикого типа) внешних сегментов фоторецепторов, клетки RPE накапливали внутриклеточные отложения липидов.
Дальнейшие тесты нокаутов ABCA4 показали признаки дефектного метаболизма липидов RPE и нарушенной способности переваривать внешние сегменты фоторецепторов, что приводит к отложению липидов в клетках RPE.
Это первое сообщение, в котором потеря функции ABCA4 в RPE человека была связана с внутриклеточными отложениями липидов в этих клетках без воздействия на внешние сегменты фоторецепторов с мутацией ABCA4. Со временем эти отложения липидов могут способствовать атрофии РПЭ, что приводит к дегенерации фоторецепторов.
«В нашем отчете представлены рекомендации по генно-терапевтическому подходу к целевому РПЭ», — сказал ведущий исследователь Капил Бхарти, доктор философии, старший научный сотрудник отдела трансляционных исследований глаз и стволовых клеток NEI. «Наши данные свидетельствуют о том, что в дополнение к коррекции потери функции ABCA4 в фоторецепторах генная терапия также должна воздействовать на клетки RPE».
Это исследование является частью более масштабных усилий NEI по решению проблемы ограниченной доступности линий стволовых клеток, полученных от пациентов, для изучения болезни Штаргардта. Чтобы преодолеть этот барьер, NEI инициировал программу сохранения STGD1-iPSC от пациентов с различными мутациями ABAC4. Эти клетки будут доступны широкому сообществу для изучения механизма и генотипа-фенотипа.
Работа финансировалась Программой внутренних исследований NEI.




















Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.