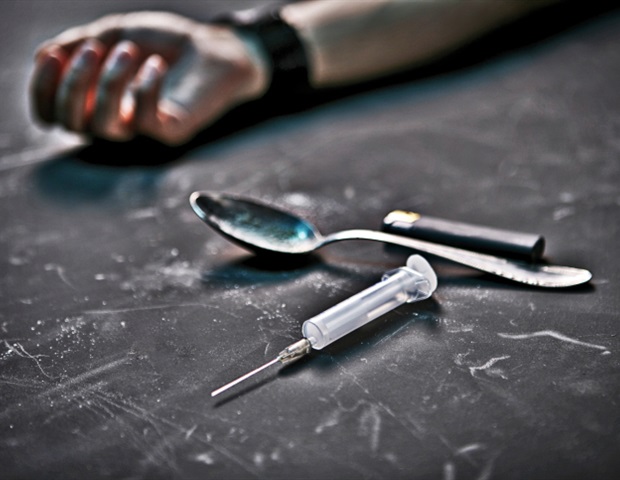
Нейробиологи из Медицинского университета Южной Каролины (MUSC) сообщают в журнале Science Advances , что звездчатые клетки мозга, известные как астроциты, могут «выключать» нейроны, участвующие в рецидиве героина. Связанные с наркотиками сигналы в окружающей среде могут усилить стремление к поиску наркотиков, что приведет к рецидиву. В этой статье группа под руководством Питера Каливаса, доктора философии, и Анны Крюер, доктора философии, оба из Департамента неврологии, изучили, как астроциты взаимодействуют с нейронами и играют ли астроциты важную роль в регуляции ответа на намеки на наркотики.
Когда мы учимся кататься на велосипеде или решать математическую задачу, клетки-посредники в нашем мозгу, известные как нейроны, создают связи, которые позволяют им лучше общаться, чтобы нам было легче выполнить ту же задачу в следующий раз. То же самое происходит, когда мы учимся ассоциировать удовольствие с вредными веществами, такими как наркотики. Нейроны посылают друг другу сильные сообщения, побуждая нас искать их снова и снова.
Связь между нейронами направляется различными клетками, особенно группой звездообразных клеток, называемых астроцитами. Астроциты окружают наши нейроны и действуют как светофоры, регулируя связь между клетками, особенно во время аддиктивного поведения.
Другим важным игроком в развитии зависимости и рецидива является глутамат – химический мессенджер. Глутамат возбуждает нейроны и заставляет их генерировать электрические сигналы для связи друг с другом. Лаборатория Каливаса сыграла ключевую роль в установлении важности глутамата. По словам Крюера, за десятилетия исследований Каливас разработал «глутаматную гипотезу зависимости».
Согласно этой гипотезе, слишком много глутамата может привести к тому, что наши нейроны будут постоянно активироваться в ответ на сигналы окружающей среды, связанные с наркотиками. Эта постоянная активация приводит к перегрузке связи между клетками, поощряя поведение, связанное с поиском наркотиков, и рецидивы.
Каливас и Крюер обнаружили, что астроциты могут замедлять сверхактивную коммуникацию.
Астроциты подобны тормозу в машине, и вы нажимаете на него, чтобы остановить сигнал глутамата».
Анна Крюер, доктор философии, кафедра неврологии, MUSC
Но как именно они это делают?
Чтобы ответить на этот вопрос, исследователи использовали хорошо зарекомендовавшую себя модель героинового рецидива. В модели крысы сначала учатся принимать героин самостоятельно, нажимая на рычаг. После нажатия рычага они получают лекарство вместе со световыми и звуковыми сигналами, что позволяет крысам ассоциировать сигналы с наркотиком. Затем сигнал и наркотик удаляются, имитируя абстиненцию. Наконец, животным снова предоставляется доступ к сигналу, и их нажатие на рычаг является мерой поиска наркотика и рецидива.
Используя этот подход, Крюер и Каливас обнаружили, что астроциты адаптируются двумя способами, чтобы уменьшить потребность в наркотиках во время отмены. Одно семейство астроцитов перемещается ближе к нейронам и отводит глутамат от синапсов, уменьшая связь между нейронами. Другое семейство увеличивает экспрессию переносчика глутамата GLT-1, который уничтожает избыток глутамата. В обоих случаях астроциты действуют как тормоз нейронной связи во время отмены.
Однако для выполнения этой тормозной функции в фазе рецидива было доступно меньшее количество астроцитов, и они располагались дальше от нейронов. Используя специальную химическую технологию, Крюер и Каливас смогли включать и выключать астроциты для изменения поведения, показывая, что эти звездообразные клетки играют важную роль.
По сути, когда астроциты окружают нейроны, — объяснила Крюер, — они поглощают глутамат и отключают этот синапс, — сказала она.
Эти результаты могут дать новое представление о том, как предотвратить рецидив.
«Поскольку астроциты в нормальном мозге подвергаются двум адаптациям для подавления рецидива, мы думаем, что они могут быть ценной клеточной мишенью для разработки терапевтических средств, нацеленных на рецидив при расстройствах, связанных с употреблением психоактивных веществ», — сказал Крюер.
Предыдущие клинические испытания показали, что одного только снижения уровня глутамата недостаточно для предотвращения рецидивов у людей. Эти данные свидетельствуют о возможности того, что комбинированный режим, который не только снижает уровень глутамата, но и усиливает эффект торможения астроцитов, может быть более успешным и требует дальнейшего изучения.
«Исторически, когда речь шла о поведенческих патологиях, все внимание уделялось нейронам», — сказал Крюер. «Наши результаты показывают, что нам необходимо более целостно взглянуть на нервную систему и учитывать, что другие типы клеток, помимо нейронов, обладают способностью влиять на поведение и могут быть ключом к лечению рецидива».
Чтобы подготовить почву для новых методов лечения на основе астроцитов, лаборатория Каливаса пытается определить потенциальные генные мишени.
«Многие гены экспрессируются в астроцитах, но не экспрессируются в других клетках мозга, включая нейроны», — сказал Каливас. «Понимание того, какие из этих генов имеют решающее значение для астроцитарной регуляции рецидива, дает нам представление о том, как разрабатывать лекарства, которые будут избирательно повышать способность астроцитов ингибировать рецидив. Это направление активных исследований в нашей лаборатории, и мы определили несколько генных продуктов, селективных к астроцитам, которые могут служить мишенями при лечении расстройств, связанных с употреблением психоактивных веществ».


















Оставить Комментарий
Ваш электронный адрес не будет опубликован. Обязательные поля помечены *