
В недавнем обзоре, опубликованном в журнале Current Opinion in Chemical Biology , исследователи обсудили последние достижения в области антимикробных свойств грудного молока.
Обзор: Последние достижения в области антимикробной активности олигосахаридов грудного молока . Кредит изображения: HTeam / Shutterstock
Фон
Человеческое грудное молоко является единственным источником питания, рекомендуемым в первые месяцы жизни новорожденного. Однако во всем мире только 40% младенцев в возрасте до шести месяцев получают грудное молоко в качестве единственного источника питания. На наблюдаемую частоту грудного вскармливания влияет множество факторов, таких как метаболические осложнения у новорожденных, осложнения со здоровьем матери, препятствующие лактации или безопасному грудному вскармливанию, и неадекватная поддержка матерей.
Грудное молоко состоит из нескольких антимикробных, противовоспалительных и иммуномодулирующих молекул, которые помогают снизить заболеваемость младенцев, установить микробиом и способствовать психомоторному и когнитивному развитию. Младенцы становятся восприимчивыми к проблемам со здоровьем в отсутствие материнского молока. В настоящем исследовании исследователи рассмотрели антимикробную активность олигосахаридов грудного молока (HMO).
ОПЗ различаются по составу.
Структурно НМО содержат пять пираноз – D-глюкозу, D-галактозу, DN-ацетилглюкозамин, N-ацетилнейраминовую кислоту и L-фукозу. Каждый олигосахарид содержит лактозу на восстанавливающем конце. К настоящему времени охарактеризовано 200 уникальных НМО, включающих от 3 до 22 моносахаридов. Состав ОПЗ варьирует у матерей и меняется в течение всей лактации. Концентрация НМО в течение лактации колеблется от 5 г/л до 25 г/л.
Состав грудного молока изменяется в соответствии с физиологическими потребностями ребенка. Первое молоко (молозиво) вырабатывается после родов до семи дней. Он почти некалориен и в первую очередь помогает установить иммунитет. К четвертой неделе рацион новорожденного включает зрелое грудное молоко. ОПЗ достигают пиковых концентраций на этой ранней стадии. Хотя матери тратят от 300 до 500 калорий на синтез НМО, они не метаболизируются, а вместо этого используются комменсальными бактериями в качестве источника углерода.
Микробиом кишечника новорожденных, не находящихся на грудном вскармливании, отличается от такового у детей, находящихся на грудном вскармливании. У детей, находящихся на искусственном вскармливании, наблюдается более высокое разнообразие микробиоты, в то время как у детей, находящихся на грудном вскармливании, в микробиоте преобладают пробиотические бифидобактерии . На более поздних стадиях лактации в микробиоме доминируют Bacteroides .
Антибактериальная активность ОПЗ

Source Naturals, OptiZinc, цинк, 240 таблеток
Streptococcus agalactiae , стрептококк группы B (GBS) и грамположительный патоген, колонизирует вагинальный тракт примерно у 15-30% здоровых женщин. Он может передаваться вертикально и вызывать неонатальный менингит и сепсис. Западные страны разработали стратегии предотвращения его передачи путем проведения пренатального скрининга на СГБ с последующей антибиотикопрофилактикой.
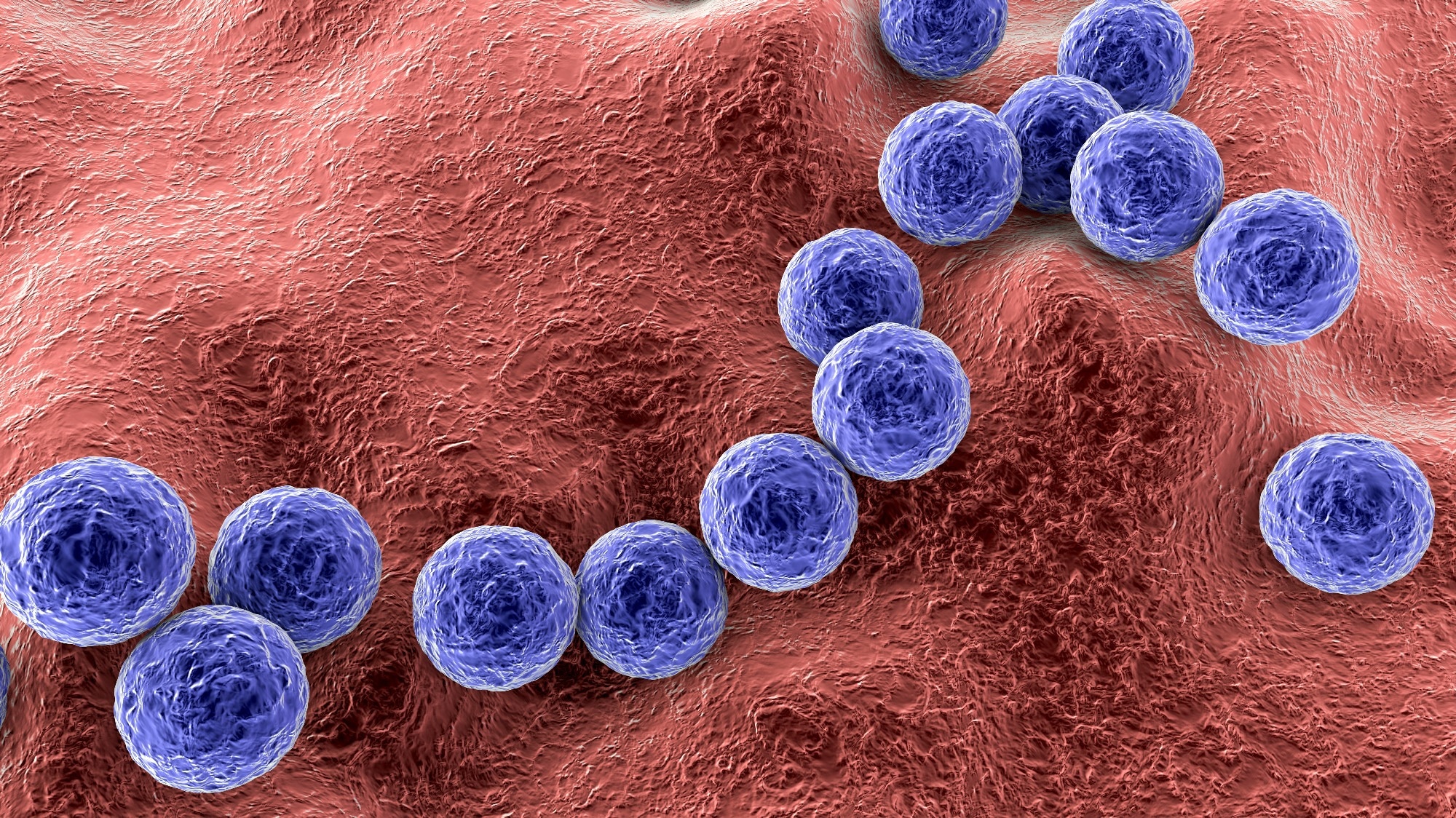
Хотя при таком подходе частота раннего начала инфекции GBS снижается, профилактической или лечебной терапии для позднего начала заболевания не существует. В качестве альтернативы исследователи изучили антимикробные свойства ОПЗ против СГБ. Одно исследование подтвердило антимикробную активность HMO против GBS и отметило, что лечение гетерогенными HMO не влияло на состав вагинальной микробиоты независимо от инфекции GBS.
HMO ингибируют образование биопленки
Бактериальные биопленки представляют собой клеточные агрегаты, заключенные в динамичный и жесткий внеклеточный матрикс (ECM), которые помогают микробам координировать свои действия в сообществе. ECM обеспечивает защиту от антибиотиков, что приводит к толерантности к антибиотикам, часто связанной с устойчивостью к противомикробным препаратам (AMR). HMO действуют как ловушки для рецепторов, подавляя прикрепление патогенов к поверхностям слизистых оболочек. Золотистый стафилококк колонизирует кожу и носоглотку у 30% населения.
Это оппортунистический возбудитель, который обычно протекает бессимптомно, но вызывает несколько клинических проявлений после установления патогенности. Известно, что эти бактерии образуют биопленки. Авторы исследования ранее сообщали об использовании ОПЗ для разрушения прикрепления бактерий к абиотическим и биотическим поверхностям. Они сообщили, что ОПЗ могут значительно ингибировать образование биопленок S. aureus .
Более того, синтетически модифицированные ГМО продемонстрировали повышенный ингибирующий эффект на образование биопленок. В другом исследовании наблюдалось снижение жизнеспособности бактериальных клеток в биопленках S. aureus , что свидетельствует о гибели клеток. Энтеропатогенные кишечные палочки (ЕРЕС) представляют собой группу серотипов кишечной палочки и известных загрязнителей воды и пищевых продуктов.
EPEC прикрепляется к кишечному эпителию и образует отдельные колонии. В ходе исследования исследователи обнаружили, что добавление HMO в культуральную среду in vitro значительно снижает прикрепление EPEC. Acinetobacter baumannii, грамотрицательный вид, широко известен своей множественной лекарственной устойчивостью (МЛУ). Инфекции, вызванные A. baumannii , возникают в отделениях интенсивной терапии (ОИТ), где пациенты имеют ослабленный иммунитет.
A. baumannii вызывает респираторную пневмонию (ВАП), при которой инфекции передаются из ее биопленок на аппаратах ИВЛ. Авторы исследования исследовали применимость ОПЗ против этого патогена, выделенного из различных анатомических областей. Они обнаружили, что HMO нарушили формирование биопленок A. baumannii , и отметили значительное снижение образования биопленок для всех протестированных изолятов.
Заключительные замечания
Учитывая растущую проблему УПП для общественного здравоохранения, исследователи изучили альтернативы терапевтическим вариантам, включая ОПЗ и другие гликозиды человеческого происхождения. Например, ОПЗ могут быть использованы благодаря их мощным противомикробным свойствам и антибиопленочным свойствам против грамположительных и грамотрицательных бактерий, включая патогены ESKAPE A. baumannii и S. aureus.

















Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.