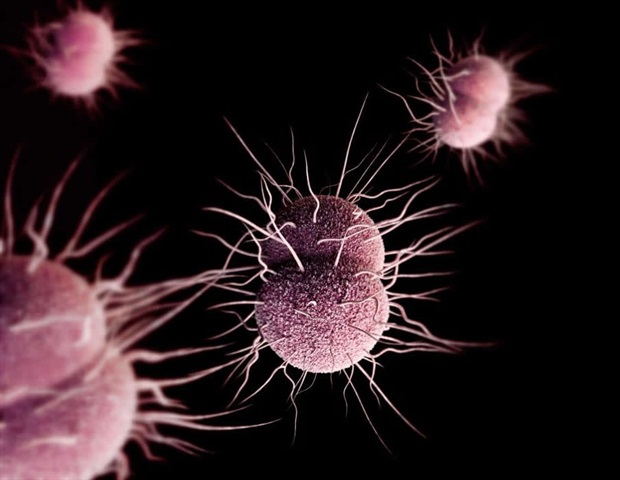
По словам исследователей из Института биомедицинских наук Университета штата Джорджия, создание мутации, подавляющей то, как бактериальный патоген Neisseria gonorrhoeae вызывает гонорею, распространенную инфекцию, передающуюся половым путем, может предложить новый способ профилактики и лечения этого заболевания.
Исследователи обнаружили, что создание мутации в ключевой части переносчика внешней мембраны, которую N. gonorrhoeae использует для захвата белков человеческого иммунитета и удаления из них металлов, может помочь предотвратить заражение гонореей. Результаты опубликованы в журнале mBio.
Гонорея, которая ежегодно поражает более 80 миллионов человек во всем мире, представляет собой глобальную угрозу для общественного здравоохранения из-за роста числа случаев устойчивости к противомикробным препаратам, роста стоимости лечения и отсутствия защитной вакцины. До 80 процентов случаев заболевания у женщин протекает бессимптомно, и при отсутствии лечения гонорея может привести к серьезным последствиям для здоровья, включая воспалительные заболевания органов малого таза, внематочную беременность, бесплодие и даже опасные для жизни эндокардит и менингит.
Эффективных вариантов лечения гонореи становится все меньше из-за развития устойчивости к противомикробным препаратам к существующим препаратам. Кроме того, сложно определить подходящие мишени для вакцины, поскольку N. gonorrhoeae изменяет экспрессию ключевых поверхностных молекул и ослабляет иммунный ответ. Чтобы помешать вторгающимся патогенам вызвать заболевание, люди полагаются на процесс, называемый пищевым иммунитетом, чтобы ограничить доступность критически важных питательных веществ, таких как железо и цинк, и морить захватчиков голодом. Белки, связывающие металлы, связывают металлы и ограничивают количество свободных основных ионов металлов, необходимых патогенам для развития и возникновения болезней.

Optimum Nutrition, Opti-Women, 120 капсул
Чтобы преодолеть усилия пищевого иммунитета хозяина, N. gonorrhoeae размещает TonB-зависимые транспортеры (TdT) на своей внешней мембране, чтобы связываться с белками пищевого иммунитета хозяина и лишать их металлов. TdT часто играют ключевую роль в развитии инфекций, что делает их многообещающими мишенями для вакцин.
Один TdT, названный TdfJ, распознает человеческий S100A7, белок, связывающий цинк, который ингибирует репликацию патогенов, скрывая цинк. N. gonorrhoeae использует TdfJ для извлечения цинка из S100A7 и усвоения металла. TdfJ содержит палец альфа-спирали во внеклеточной петле 3. Аналогичная альфа-спираль в петле 3 другого гонококкового TdT, известного как TbpA, играет критическую роль во взаимодействии между TbpA и человеческим трансферрином, который необходим для поглощения железа. . Основываясь на этой информации, исследователи предположили, что спираль 3 петли TdfJ (L3H) участвует во взаимодействиях с S100A7, и они произвели серию мутаций в L3H TdfJ, чтобы определить, блокируют ли они способность N. gonorrhoeae усваивать цинк и, следовательно, вызвать заболевание.
«Перспектива неизлечимых гонококковых инфекций подстегнула усилия по определению мишеней для новых терапевтических и профилактических стратегий, и члены семейства TonB-зависимых переносчиков металлов внешней мембраны стали перспективными кандидатами, поскольку они играют решающую роль в установлении инфекции», — говорится в исследовании. Доктор Синтия Нау Корнелиссен, старший автор исследования, заслуженный профессор университета и директор Центра трансляционной иммунологии в Институте биомедицинских наук штата Джорджия. «Наше исследование показало, что мутагенез ключевых остатков в TdfJ L3H снижает связывание S100A7 и пиратство цинка гонококком, при этом наиболее выраженные эффекты наблюдаются при заменах в остатках K261 и R262. В совокупности эти данные предполагают ключевую роль TdfJ L3H. в подрыве пищевого иммунитета хозяина.
Исследование охарактеризовало связывающее взаимодействие между импортером цинка TdfJ и его источником цинка человека, S100A7, а также определило ключевую область TdfJ, которая опосредует это взаимодействие.
Мы впервые подробно описали взаимодействие связывания гонококкового TdfJ и его человеческого лиганда S100A7. Мы также идентифицировали несколько мутаций в петле 3 TdfJ, которые изменяют связывание S100A7 и последующую экстракцию цинка. Обладая более глубоким пониманием сложных взаимосвязей между этими бактериальными рецепторами питательных веществ и их источниками питательных веществ, мы можем помочь проложить путь к определению эффективной профилактики и/или лечения важного заболевания человека».
Ставрос А. Мауракис, первый автор и доктор философии. Выпускник Института биомедицинских наук штата Джорджия.
Соавторами исследования являются Ставрос А. Мауракис, Джули Л. Стауденмайр и Синтия Нау Корнелиссен из Института биомедицинских наук штата Джорджия; и Джеффри К. Раймер и Уолтер Дж. Чазин из Университета Вандербильта.
Исследование финансируется Национальным институтом здравоохранения (NIH).





















Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.