В недавнем исследовании, опубликованном на сервере bioRxiv *, исследователи из Медицинского научно-исследовательского института инфекционных заболеваний армии США оценили иммуногенность вакцины дезоксирибонуклеиновой кислоты (ДНК) против коронавируса тяжелого острого респираторного синдрома 2 (SARS-CoV-2), nCOV- S(JET) у макак-резусов. Предыдущая оценка ДНК-вакцины против этой коронавирусной болезни 2019 (COVID-19), нацеленной на шиповидный белок (S) SARS-CoV-2, вызвала адекватный гуморальный иммунный ответ у сирийских хомяков.
Исследование: гуморальная иммуногенность ДНК-вакцины против коронавирусной болезни 2019 (COVID-19) у макак-резусов (Macaca mulatta), доставляемая с помощью безыгольной струйной инъекции.
Об исследовании
В текущем исследовании исследователи предположили, что nCOV-S (JET) будет вызывать обнаруживаемый ответ нейтрализующих антител при доставке с помощью безыгольной струйной инъекции, и искали доказательства его иммуногенности на макаках-резусах, модели приматов, отличных от человека (NHP).
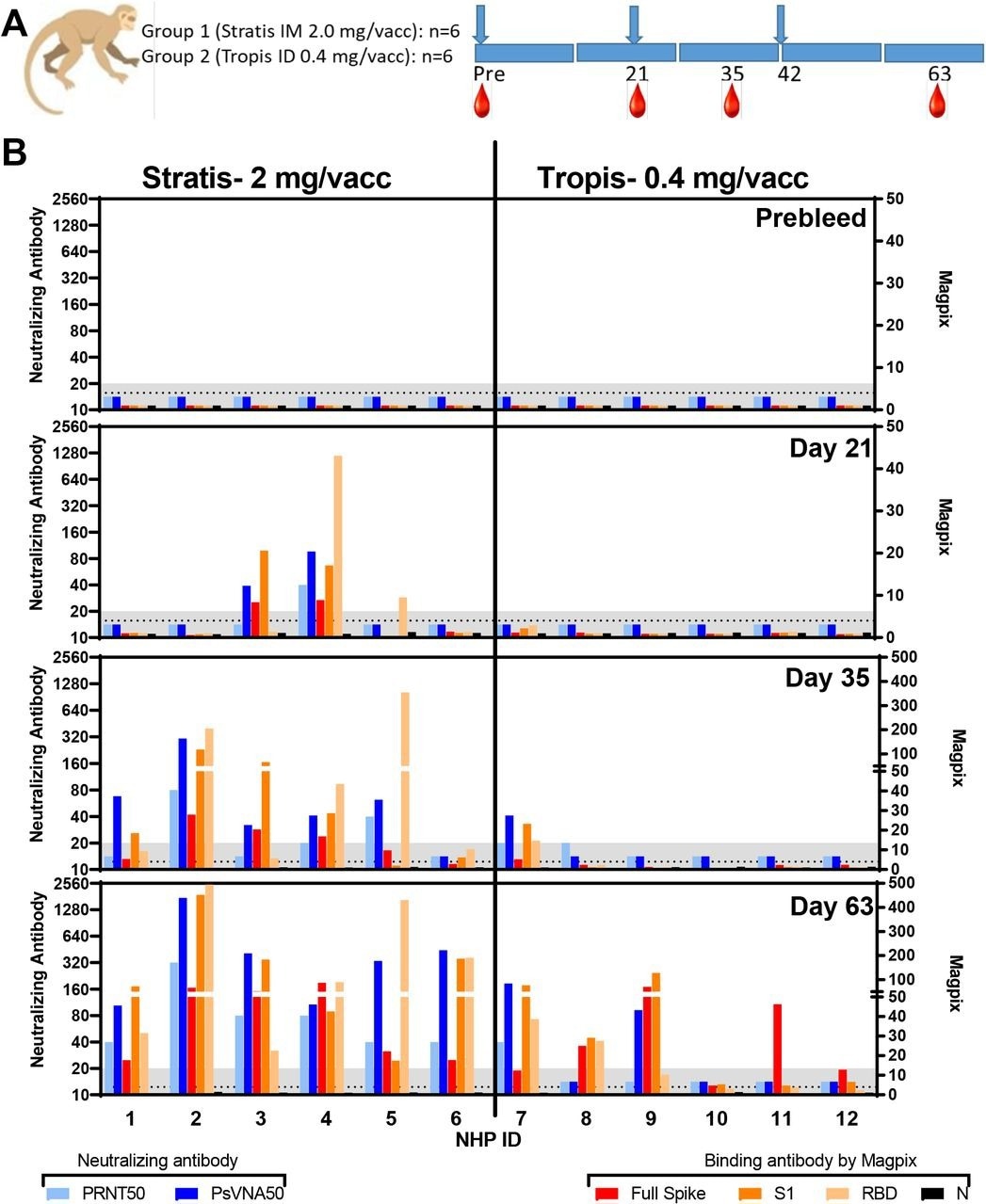
Они вакцинировали подопытных животных двумя безыгольными методами. Первым использованным методом было устройство Stratis для внутримышечной (IM) доставки 2 мг на дозу вакцины. Вторая попытка внутрикожной (ID) доставки 0,4 мг на вакцинацию с помощью устройства Tropis. Устройства Stratis и Tropis доставляли вакцины в виде струи жидкости внутримышечно или внутрикожно соответственно. Команда измерила нейтрализующие антитела, вызванные вакциной, с помощью двух анализов: i) тесты нейтрализации уменьшения бляшек живого вируса (PRNT); ii) анализы нейтрализации псевдовирионов (PsVNA). Кроме того, они провели мультиплексный иммуноанализ MAGPIX, в котором используются белки SARS-CoV-2 S, S1, рецептор-связывающий домен (RBD) и нуклеокапсид (NP).
В исследовании приняли участие 12 макак-резусов китайского происхождения в возрасте от восьми до 15 лет и весом от пяти до 16 килограммов. Каждая группа вакцинации включала случайно выбранных трех самцов и трех самок животных. Команда вакцинировала всех подопытных животных в нулевой, 21-й и 42-й дни и собрала у них образцы цельной крови в нулевой, 21-й, 35-й, 63-й и 168-й дни. Они ежедневно контролировали всех подопытных животных на наличие клинических и поведенческих аномалий.
Результаты исследования
Макакам-резусам потребовалась дополнительная (вторая) стимуляция, чтобы достичь таких же титров нейтрализующих антител, как у сирийских хомяков. Среднегеометрический титр (СГТ) или PsVNA50 у хомяков после двух вакцинаций составлял приблизительно 640, тогда как у макак-резусов он равнялся 58 и 326 после двух и трех вакцинаций соответственно. Точно так же GMT PRNT50 у хомяков после двух вакцинаций составлял примерно 640, тогда как у макак-резусов он составлял 24 и 71 после двух и трех вакцинаций соответственно.

Kyolic, Aged Garlic Extract, выдержанный экстракт чеснока с лецитином, 200 капсул
Примечательно, что ДНК-вакцины проявляют наибольшую иммуногенность при в/м введении по сравнению с другими путями. В то время как хомяки получили в общей сложности 0,4 мг nCOV-S (JET) внутримышечно в течение трех вакцинаций, NHP получили дозу в шесть мг, что означает, что NHP получили неадекватную дозу по сравнению с хомяками в расчете на вес.
Тем не менее, эта ДНК-вакцина, введенная с помощью иглы, защищала НЧП от болезней. Он вызывал титры нейтрализующих антител более 100 при измерении с помощью PsVNA. В другом исследовании была протестирована аналогичная ДНК-вакцина на основе S, названная ZyCoV-D, на кроликах. Три дозы его внутрикожной доставки с использованием устройства Tropis вызывали титр нейтрализующих антител 108, что оценивалось с помощью теста микронейтрализации. Таким образом, титры нейтрализующих антител, индуцированные у NHP, кажутся сравнимыми с титрами, которые были защитными у кроликов.
Кроме того, согласно оценке PsVNA, вакцина nCOV-S(JET), доставляемая с помощью устройства IM Stratis, проявляла перекрестную нейтрализующую активность в отношении вызывающих озабоченность вариантов SARS-CoV-2 (VOC). Все NHP имели минимальный титр PsVNA50 80 против штамма SARS-CoV-2 WA-1, бета- и дельта-ЛОС. Примечательно, что титры нейтрализующих антител против Delta VOC были самыми высокими.
Напротив, ДНК-вакцина, доставляемая внутривенно с помощью устройства Tropis, имела более низкие реакции перекрестной нейтрализации ЛОС. Только у двух животных (№ 7 и № 9) были обнаружены перекрестно-нейтрализующие антитела против всех ЛОС, измеренные с помощью PsVNA, и только у № 7 были обнаружены обнаруживаемые перекрестно-нейтрализующие антитела против всех летучих органических соединений, протестированных с помощью PRNT. Животные № 7 и № 9 также имели наиболее устойчивый ответ связывания антител, измеренный с помощью Magpix. Среди других преимуществ ДНК-вакцина nCOV-S(JET) не содержала липидных наночастиц (ЛНЧ) и не требовала адъюванта или электропорации. Просто использовались относительно недорогие одноразовые безыгольные шприцы.
Выводы
Будущие исследования должны изучить способы повышения эффективности ДНК-вакцины nCOV-S (JET), чтобы ее можно было использовать в качестве отдельной вакцины. Однако для дозировок, использованных в текущем исследовании, она вызывала желаемые реакции нейтрализующих антител после двухдозового режима, что делает эту вакцину наиболее полезной для стратегий гетерологичной бустерной иммунизации. В этой стратегии вакцинации используется бустерная вакцина с платформы, отличной от той, которая использовалась для завершения серии первичной вакцинации.
Несколько исследований показали, что гетерологичные бустеры вызывают аналогичную реактогенность и большую иммуногенность, чем гомологичные бустеры для всех комбинаций. Поэтому еще 21 октября 2021 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) разрешило использование вакцин мРНК-1273, Ad26.COV2.S и BNT162b2 против COVID-19 в качестве гетерологичных бустеров. Аналогичным образом, системный обзор показал, что гетерологичное праймирование BNT162b2 обеспечивает надежную иммуногенность и приемлемую реактогенность. Тем не менее, необходимы дополнительные исследования для установления оптимальных комбинаций, режимов дозирования и долгосрочных профилей безопасности гетерологичных стратегий вакцинации. Подводя итог, текущее исследование подтвердило иммуногенность ДНК-вакцины nCOV-S(JET) и показало ее способность вызывать быстрый гуморальный иммунный ответ при НГП.
*Важное замечание
bioRxiv публикует предварительные научные отчеты, которые не рецензируются экспертами и, следовательно, не должны рассматриваться как окончательные, направляющие клиническую практику/поведение, связанное со здоровьем, или рассматриваться как установленная информация.





















Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.