
В недавнем исследовании, опубликованном на сервере препринтов bioRxiv *, исследователи из США оценили роль двух цитокинов, интерферона-гамма (IFN-γ) и интерлейкина-10 (IL-10), в регуляции иммунных клеточных ответов и раннего воспаления. во время тяжелого острого респираторного синдрома коронавирусной инфекции 2 (SARS-CoV-2) у макак-резусов.
Исследование: ИЛ-10 подавляет размножение Т-клеток, одновременно способствуя образованию резидентных клеток памяти во время инфекции SARS-CoV-2 у макак-резусов.
Фон
В то время как IFNγ является провоспалительным цитокином, IL-10 является противовоспалительным цитокином. Эти два различных пути определяют баланс воспаления и репликации SARS-CoV-2 в начале коронавирусной болезни 2019 (COVID-19) или на ее ранних стадиях. Однако исследования почти не изучали значение этих цитокинов во время инфекции SARS-CoV-2.
Об исследовании
В настоящем исследовании исследователи использовали модель нечеловекообразных приматов (NPH) для измерения изменений в воспалении легких, репликации вируса и клеточных иммунных реакциях против SARS-CoV-2 после блокирования цитокиновых путей. Исследование имело заранее определенную конечную точку между 28 и 35 днями после заражения.
Команда создала три экспериментальные группы, каждая из которых включала пять самцов макак-резусов в возрасте от 2,5 до 5 лет и весом от 3,5 до 5 кг. Они заразили подопытных животных SARS-CoV-2 пятью волнами, при этом каждая волна заражения заражала одно животное на группу лечения (всего три).

NutriBiotic, назальный спрей, 29,5 мл (1 жидк. унция)
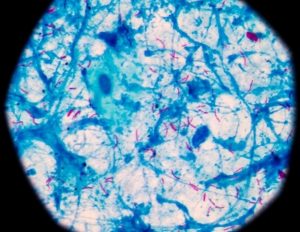
Исследователи использовали репортерные клеточные линии HEK-BlueTM для количественной оценки передачи сигналов IL-10 и IFNγ in vitro. Реакция изменения цвета указывала на величину передачи сигналов цитокинов, которую команда количественно оценила с помощью спектрофотометра при длине волны 650 нанометров. Они использовали ф-фтордезоксиглюкозу (ФДГ)-позитронно-эмиссионную томографию (ПЭТ)/компьютерную томографию (КТ) для визуализации грудной клетки инфицированных макак. Они определили интересующие объемы (VOI) или поражения в каждом сканировании органов грудной клетки, полученном на 2-й или 6-й день, которые они перенесли на совмещенные изображения ПЭТ/КТ для оценки изменения объема поражения или поглощения ФДГ.
Во время вскрытия животных команда обрабатывала очаги поражения, которые на ПЭТ/КТ казались непрерывными, но возникали в результате воспаления более чем в одной доле легкого по отдельности. Кроме того, они сканировали верхнюю часть живота, включая селезенку и поперечную ободочную кишку, а также голову и шею. Это помогло им определить поглощение (18F)ФДГ миндалинами и носовыми раковинами.
Наконец, исследователи собрали легкие и прилегающие к ним дыхательные пути, носовые раковины, слюнные железы, миндалины, селезенку, ткани и лимфатические узлы умерщвленных животных. В легких они оценили локализацию Т-клеток в паренхиме, тогда как они использовали ткани лимфатических узлов для выделения рибонуклеиновой кислоты (РНК), гистологического анализа и препаратов одиночных клеток для проточной цитометрии.
Результаты исследования
Хотя блокада IFNγ снижала образование зародышевых центров в реактивных лимфатических узлах, она практически не влияла на какие-либо особенности В- или Т-клеточного ответа. Исследователи не оценивали какое-либо возможное влияние IFNγ на функцию миелоидных клеток, даже если оно было. Тем не менее, они обнаружили некоторые интересные эффекты IL-10 на специфические для SARS-CoV-2 ответы Т-клеток.
Во-первых, IL-10 ингибировал величину вирусспецифических ответов Т-клеток в кровообращении, нижних дыхательных путях и легочных лимфатических узлах. Анализ экспрессии гена маркера пролиферации Ki-67 подтвердил, что IL-10 не продлевает циклирование вирусспецифических Т-клеток, а опосредует их во время ранней клональной вспышки. Во-вторых, ИЛ-10 повышал скорость, с которой Т-клетки, специфичные для SARS-CoV2, дифференцировались в тканерезидентные Т-клетки памяти (TRM) на поверхности слизистых оболочек нижних дыхательных путей, вероятно, за счет активации моноцитов для увеличения продукции фактора некроза опухоли бета. (TGFβ), что, в свою очередь, способствует фенотипу клеток TRM.
Удивительно, но макаки-резусы не показали специфических для SARS-CoV-2 Т-клеточных ответов в слизистой оболочке носа. Фактически блокада IL-10 уменьшала количество клеток TRM в их слизистой оболочке носа. Однако исследования на мышах обнаружили в слизистой оболочке носа клетки TRM, специфичные для SARS-CoV-2. Данные исследования указывают на возможность того, что увеличение IFΝγ может привести к усилению контроля над репликацией SARS-CoV-2. Аналогичным образом введение экзогенного IL-10 во время вакцинации слизистых оболочек может способствовать образованию резидентных в тканях Т-клеток памяти. Другими словами, данные исследования могут иметь значение для использования этих цитокинов в качестве адъювантов для вакцинации против COVID-19. Авторы предупредили, что результаты исследования были ограничены условиями легкой формы COVID-19, а IFNγ и IL-10 могут играть разные функциональные роли во время тяжелой формы COVID-19. Будущие исследования с использованием моделей NHP пневмонии COVID-19 могут пролить свет на клеточные и молекулярные механизмы иммуноопосредованного повреждения легких.
Выводы
Результаты исследования показали, что оба цитокина, IFNγ и IL-10, не играли критической роли в контроле репликации SARS-CoV-2 на модели макаки-резуса. Блокада IFNγ в некоторой степени уменьшала воспаление легких, но не влияла на врожденные лимфоциты, нейтрализующие антитела или антигенспецифические Т-клетки. С другой стороны, блокада ИЛ-10 временно усиливала воспаление легких, подавляла накопление Т-клеток, специфичных для SARS-CoV-2, в нижних дыхательных путях и способствовала ТРМ на поверхностях слизистых оболочек дыхательных путей. Поскольку эти цитокины существенно не влияли на вирусную нагрузку, инфекция SARS-CoV-2 у всех подопытных животных в конечном итоге разрешилась.
*Важное замечание
bioRxiv публикует предварительные научные отчеты, которые не рецензируются экспертами и, следовательно, не должны рассматриваться как окончательные, направляющие клиническую практику/поведение, связанное со здоровьем, или рассматриваться как установленная информация.























Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.