По состоянию на 18 октября 2022 года более 625 миллионов человек во всем мире инфицированы коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2), возбудителем коронавирусной болезни 2019 (COVID-19).
Исследование: повышенный уровень воспалительных молекул в крови пациентов с длительным COVID указывает на тромботический эндотелиит. Изображение предоставлено: Дай Йим / Shutterstock.com
Введение
Многие выжившие испытывают долгосрочные симптомы в течение нескольких месяцев после клинического разрешения вирусной инфекции. Это называется постострыми последствиями COVID-19 (PASC) или длительным Covid.
Было предложено шесть механизмов длительных симптомов COVID , которые включают персистенцию SARS-CoV-2, гиперактивацию тромбоцитов и образование микросгустков, образование аутоантител, нарушение регуляции иммунитета, полиорганную дисфункцию и реактивацию SARS-CoV-2 из-за покой.
Новое исследование, опубликованное на сервере препринтов medRxiv* , определяет, как активация эндотелия и воспаление способствуют образованию микротромбов при PASC.
Активация тромбоцитов и фибриналоидные микросгустки
В более ранних сообщениях описывалось наличие микросгустков в кровотоке пациентов с длительным Covid. Эти микросгустки, которые сопротивляются нормальному разрушению сгустка за счет фибринолиза, состоят из амилоида фибрина и могут возникать в результате активации плазмы шиповидным белком SARS-CoV-2 .
Внутри этих микротромбов находится множество захваченных воспалительных химических веществ, таких как альфа-2-антиплазмин (α2AP), различные цепи фибриногена, фактор фон Виллебранда (vWF), тромбоцитарный фактор 4 (PF4), сывороточный амилоид A (SAA) и различные антитела. Таким образом, острая коагулопатия характеризует острое тяжелое течение COVID-19.
Без разрешения этого процесса стойкая и токсическая гипоксия и плохой кислородный обмен на тканевом уровне могут вызвать затяжное повреждение. Недавний отчет показал более высокую, чем ожидалось, частоту образования тромбов и других сосудистых событий на срок до 49 недель от начала острой инфекции.
Опубликованные на данный момент данные указывают на широко распространенное воспаление эндотелия, а его основными причинами являются неисправная (неадекватная) фибринолитическая система и персистирующая коагулопатия ».
Об исследовании
В текущем исследовании выявлены маркеры в растворимой фракции крови, в отличие от твердых компонентов, которые могут помочь подтвердить роль эндотелиальной патологии и коагулопатии при длительном COVID.
Биомаркеры были выбраны из более ранних отчетов, в которых они были описаны как захваченные микросгустками, и включали vWF, PF4, SAA и α-2AP. Кроме того, были проанализированы маркеры повреждения эндотелия, в том числе молекула адгезии эндотелиально-лейкоцитарных клеток 1 (E-селектин) и молекула адгезии эндотелиальных клеток тромбоцитов 1 (PECAM-1).

California Gold Nutrition, Органическая спирулина, 500 мг, 720 таблеток
Каждая из этих молекул высвобождается во время эндотелиальной активации или аномальной активации путей свертывания крови. Некоторые из них, такие как α-2AP, нарушают фибринолиз, что приводит к тромбозу микрососудов вокруг аномальных сгустков и увеличивает риск тромбоэмболии. Эта молекула уже является прогностическим маркером неблагоприятных исходов у пациентов с сердечно-сосудистыми заболеваниями.
Маркеры эндотелиальной дисфункции были выбраны из-за центральной роли этого феномена при длительном течении COVID. В дополнение к поиску увеличения этих соединений при длительном COVID, ученые исследовали их участие в белок-белковых взаимодействиях с белками плазмы, чтобы вызвать образование микросгустков, и с рецепторами тромбоцитов, чтобы вызвать гиперактивацию тромбоцитов.
Что показало исследование?
Все шесть молекул присутствовали на более высоких средних уровнях у пациентов с длительным течением COVID по сравнению с другими, что подтверждает более ранние исследования.
В частности, уровни α-2AP превышали верхние нормальные пределы, при этом средние уровни других пяти молекул в образцах, взятых у пациентов с длительным течением COVID, были повышены по сравнению с контрольной группой. Исследователи предполагают, что фактические уровни, вероятно, намного выше.
Это вызывает тревогу, если принять во внимание, что ранее было показано, что значительная часть общего количества этих воспалительных молекул заключена в устойчивых к фибринолизу микросгустках (таким образом снижая видимый уровень растворимых молекул ).
Эти молекулы опосредуют воспаление и активацию тромбоцитов, вызывая повреждение эндотелия и обширное повреждение сосудов. Текущее исследование дополнило эти знания, показав, как их концентрации в растворимой фракции плазмы повышались у пациентов с длительным течением COVID.
Шесть маркеров участвуют в различных процессах коагуляции. Например, vWF запускает внутрисосудистую активацию и агрегацию тромбоцитов, что приводит к тромбозу из-за связывания с фибриногеном. Кроме того, SAA связывается с несколькими молекулами внеклеточного матрикса и эндотелиальными толл-подобными рецепторами (TLR), впоследствии способствуя высвобождению медиаторов воспаления и активных форм кислорода (АФК).
Возникающее в результате повреждение эндотелия связано с функциональным нарушением этой ткани и ранним образованием атеромы. Этот процесс также активирует инфламмасому NLRP3, вызывая образование тромбина путем активации каскада коагуляции.
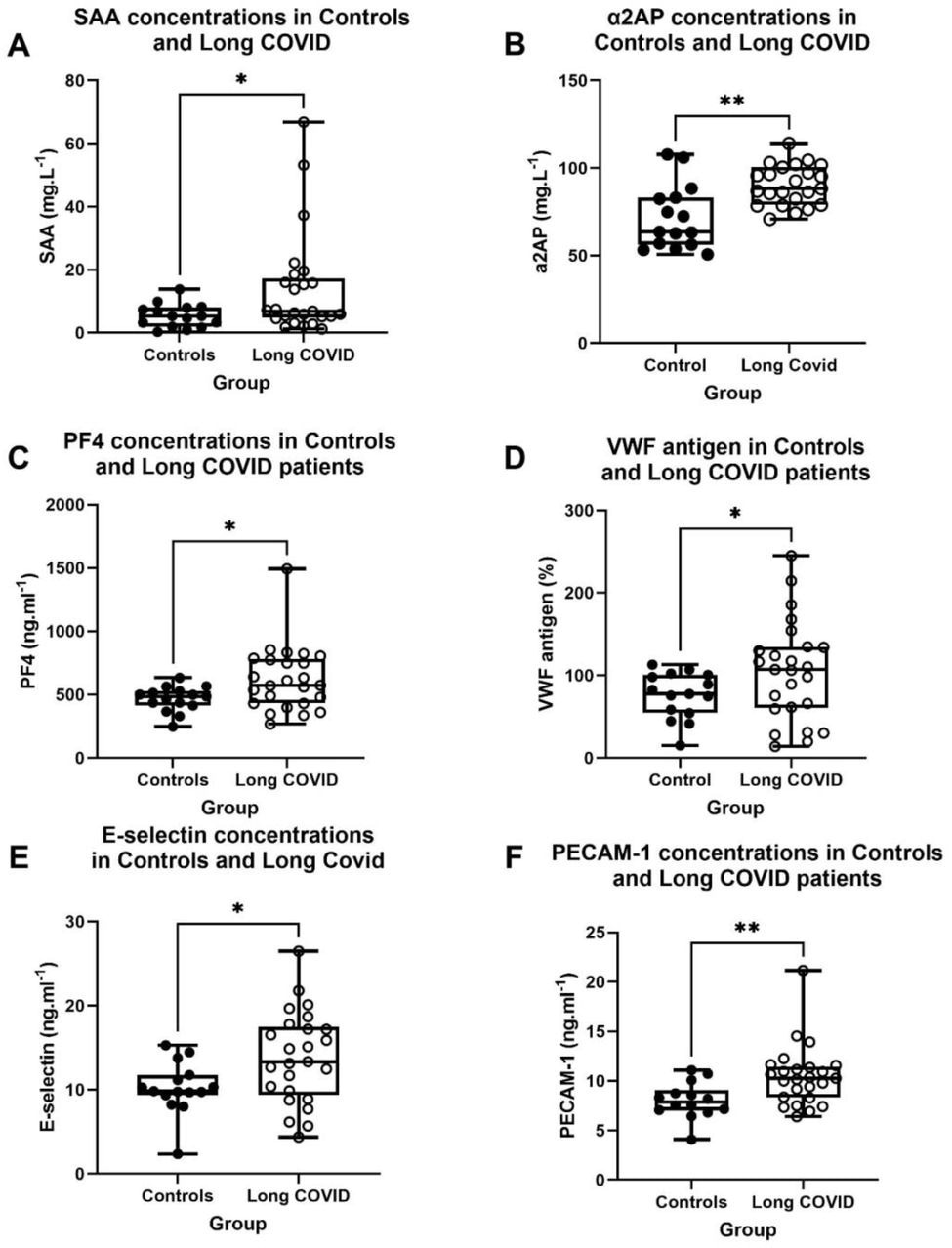
Концентрация воспалительных молекул [или % антигена в случае фактора фон Виллебранда (VWF)] в контроле и при длительном COVID в системном кровотоке. (A) SAA-, (*p<0,05), (B) α2AP- (**p<0,01), (C) PF4- (*p<0,05) и (D) концентрации фактора Виллебранда в контроле и Long COVID с использованием PPP (*р<0,05). (Д) Е-селектин-и (**р<0,01). (F) Концентрации PECAM-1 в контроле и Long COVID с использованием сыворотки (*p<0,05). Сокращения: SAA: сывороточный амилоид A, α-2AP: α-2 антиплазмин, PF4: фактор тромбоцитов 4, VWF: фактор фон Виллебранда, E-селектин: молекула адгезии эндотелиально-лейкоцитарных клеток 1, PECAM-1: молекула адгезии эндотелиальных клеток тромбоцитов-1, PPP: Бедная тромбоцитами плазма.
Повышенные уровни α-2AP заставляют микротромбы сопротивляться фибринолизу за счет связывания с плазмином, обладающим фибринолитическими свойствами. Это вызывает образование тромбов в артериях и венах, эмболию и ишемический инсульт.
Повышенные уровни Е-селектина также подтверждают активацию эндотелия. Эта молекула привязывает лейкоциты к эндотелиальным клеткам, позволяя им катиться по активированному эндотелию и, в конечном счете, запуская адгезию тромбоцитов к эндотелию.
Сообщалось, что E-селектин и PECAM-1 вызывают микротромбы и гиперактивацию тромбоцитов в образцах крови здоровых пациентов, о чем также сообщалось в предыдущих образцах, полученных от пациентов с длительным течением COVID. Эти события могут быть связаны с белок-белковыми взаимодействиями с белками плазмы, которые вызывают неправильное сворачивание, и с рецепторами тромбоцитов, которые приводят к гиперактивации.
Выводы
Нарушение коагуляции, способствующее ишемически-реперфузионному повреждению за счет образования резистентных к фибринолизу фибрин-амилоидных микросгустков, является ключевым механизмом, ответственным за развитие затяжного COVID. Это подтверждается наличием таких сгустков и относительно повышенными уровнями шести медиаторов воспаления, которые играют жизненно важную роль в коагуляции и активации эндотелия.
Распространенным патологическим процессом является тромботический эндотелиит [включающий] аномальные фибриналоидные микросгустки, гиперактивированные тромбоциты, эндотелиит и повышенный уровень протромботических воспалительных молекул, которые взаимодействуют друг с другом, а также с тромбоцитами и эндотелием ».
*Важное замечание
medRxiv публикует предварительные научные отчеты, которые не рецензируются экспертами и, следовательно, не должны рассматриваться как окончательные, направляющие клиническую практику/поведение, связанное со здоровьем, или рассматриваться как установленная информация.





















Leave a Comment
Your email address will not be published. Required fields are marked with *