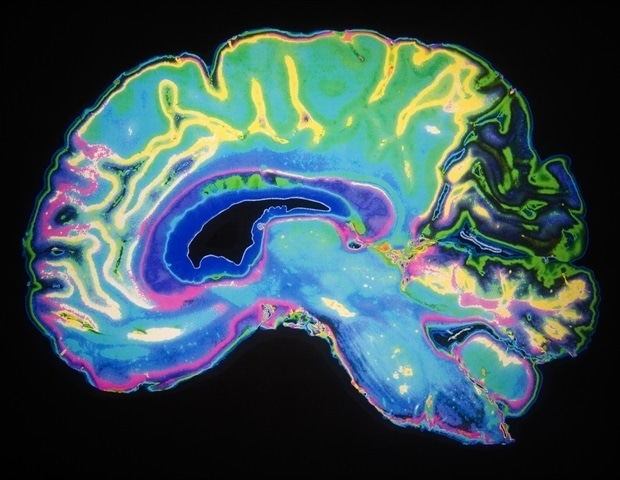
Используя стволовые клетки для выращивания в лаборатории миниатюрных мозгоподобных органов, ученые открыли новые возможности для изучения неврологического развития, болезней и методов лечения, которые невозможно проводить на живых людях. Но не все органоиды мини-мозга созданы одинаковыми, и заставить их точно имитировать ткани человеческого мозга, которые они моделируют, было постоянной проблемой.
Прямо сейчас это похоже на Дикий Запад, потому что не существует стандартного метода создания органоидов мини-мозга. Каждый нейробиолог хочет создать органоидную модель своего любимого заболевания, но все же органоиды не всегда выглядят одинаково».
Беннет Нович, член Центра регенеративной медицины и исследований стволовых клеток Эли и Эдит Броуд в Калифорнийском университете в Лос-Анджелесе и старший автор новой статьи.
Фактически, из-за отсутствия общего протокола для их производства и отсутствия руководств по контролю качества органоиды могут варьироваться от лаборатории к лаборатории; и даже от партии к партии -; это означает, что открытие, сделанное в одном органоиде, может оказаться неверным в другом.
«Если бы моя лаборатория и другая лаборатория, расположенная дальше по коридору, проводили тесты на наркотики с использованием мини-мозговых органоидных моделей одного и того же расстройства, мы все равно могли бы получить разные результаты», — говорит Момоко Ватанабе, первый автор новой статьи и доцент кафедры анатомии и анатомии. нейробиологии в Калифорнийском университете в Ирвине. «Мы не будем знать, чьи выводы верны, потому что наблюдаемые нами различия могут быть отражением различий наших моделей, а не отражением болезни».
В своем новом исследовании, опубликованном сегодня в Stem Cell Reports, Нович, Ватанабэ и их коллеги предлагают рекомендации, основанные на их исследованиях, которые могут помочь ученым преодолеть два основных препятствия, стоящих на пути полного потенциала этих органоидов: различия в однородности и структуре.
Наличие органоидов, которые точно и последовательно воссоздают структуру и клеточный состав определенных отделов мозга, особенно важно для изучения таких расстройств, как шизофрения и расстройства аутистического спектра, при которых мозг пораженных людей часто выглядит идентичным нейротипическому мозгу по структуре, но демонстрирует заметные различия в структуре. функция.
«Мы никогда не сможем идентифицировать тонкие различия в структуре и функциях мозга — то, что важно для пациентов с неврологическими расстройствами — если наши органоиды имеют неправильный баланс типов клеток или грубо неправильную структуру», — сказал Нович, который также является директором Интегрированного центра восстановления нервной системы Калифорнийского университета в Лос-Анджелесе.
Создание лучших органоидов: вопрос зрелости
Чтобы получить органоиды мини-мозга, диаметр которых может варьироваться от 1 до 5 миллиметров, ученые сначала берут клетки кожи или крови человека и перепрограммируют их, чтобы они стали индуцированными плюрипотентными стволовыми клетками ; клетки, которые могут дифференцироваться в любой тип клеток в организме. Затем они направляют эти iPS-клетки на создание нервных стволовых клеток, которые могут производить большинство типов клеток, обнаруженных в мозге. По мере формирования нейральных стволовых клеток их можно уговорить агрегировать в трехмерные органоиды. Достаточно просто. Но почему одни органоиды больше похожи на человеческий мозг, чем другие?
Чтобы ответить на этот вопрос, команда сотрудничала с экспертами по плюрипотентности Кэтрин Плат и Амандер Кларк из Центра исследования стволовых клеток Калифорнийского университета в Лос-Анджелесе. Они обнаружили, что зрелость стволовых клеток, из которых выращен органоид, влияет на его качество так же, как свежесть ингредиентов влияет на качество кулинарного блюда.
«В эмбриональном развитии человека нервная система формируется одной из первых структур, поэтому вполне логично, что стволовые клетки, которые находятся на ранних стадиях развития, лучше всего производят органоиды головного мозга», — сказал Ватанабэ, который также является членом UCI Sue. и Исследовательский центр стволовых клеток Билла Гросса.
Затем исследователи обнаружили, что лучший способ сохранить человеческие стволовые клетки на раннем этапе развития, подходящем для образования органоидов, — это вырастить их в чашке с клетками кожи мыши, называемыми питателями фибробластов, поскольку они обеспечивают важные химические сигналы и структурную поддержку, которые помогает стволовым клеткам расширяться и сохранять свою незрелость с течением времени.
К сожалению, они также обнаружили, что использование клеток мыши может сделать органоиды менее подходящими для разработки клеточной терапии для замены больных или поврежденных нервных тканей. Кроме того, эти методы с фидерной поддержкой более трудоемки, чем методы выращивания стволовых клеток, обычно используемые во многих лабораториях.
Затем команда обратилась к секвенированию РНК и компьютерному анализу, пытаясь определить генетические различия между стволовыми клетками, которые производят хорошие органоиды, и теми, которые этого не делают. Это позволило им идентифицировать четыре молекулы -; все принадлежащие к надсемейству молекул трансформирующего фактора роста бета — ; которые отвечали за сохранение стволовых клеток в менее развитом состоянии.
Добавление этих четырех молекул к стволовым клеткам, растущим в чашке, удерживало их в незрелом состоянии и позволяло этим клеткам производить высококачественные, хорошо структурированные органоиды.
«Мы нашли способ не только съесть свой пирог, но и съесть его», — сказал Нович. «Мы убрали мышиные клетки из уравнения, сохранив при этом некоторые из их преимуществ для формирования органоидов, что приблизило нас к нашим целям изучения и разработки методов лечения сложных неврологических заболеваний».
Исследование финансировалось программой Ablon Scholars Program в Комплексном онкологическом центре Йонссона Калифорнийского университета в Лос-Анджелесе и Широком исследовательском центре стволовых клеток; награды за исследования и обучение от Национальных институтов здравоохранения, Калифорнийского института регенеративной медицины, Фонда Роуз-Хиллз и Широкого исследовательского центра стволовых клеток; Мемориальный фонд Уэхары; Институт исследования мозга Калифорнийского университета в Лос-Анджелесе; и стипендия факультета от Медицинского института Говарда Хьюза.
























Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.