По состоянию на 27 сентября 2022 года коронавирусная болезнь 2019 года (COVID-19) стала причиной более 6,5 миллионов смертей во всем мире. Вызванный коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2), COVID-19 был на удивление непредсказуемым по своей клинической тяжести.
В результате было предпринято много усилий для определения факторов, повышающих индивидуальный риск тяжелого или летального исхода COVID-19. В недавнем исследовании журнала Pathogens рассматривается потенциальная роль микробиома кишечника в определении тяжелой формы COVID-19.
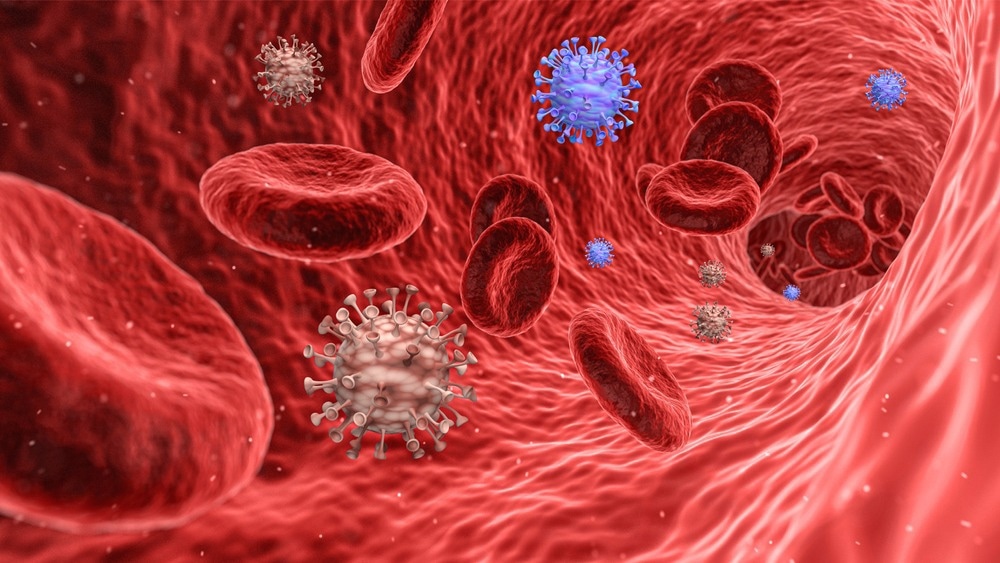
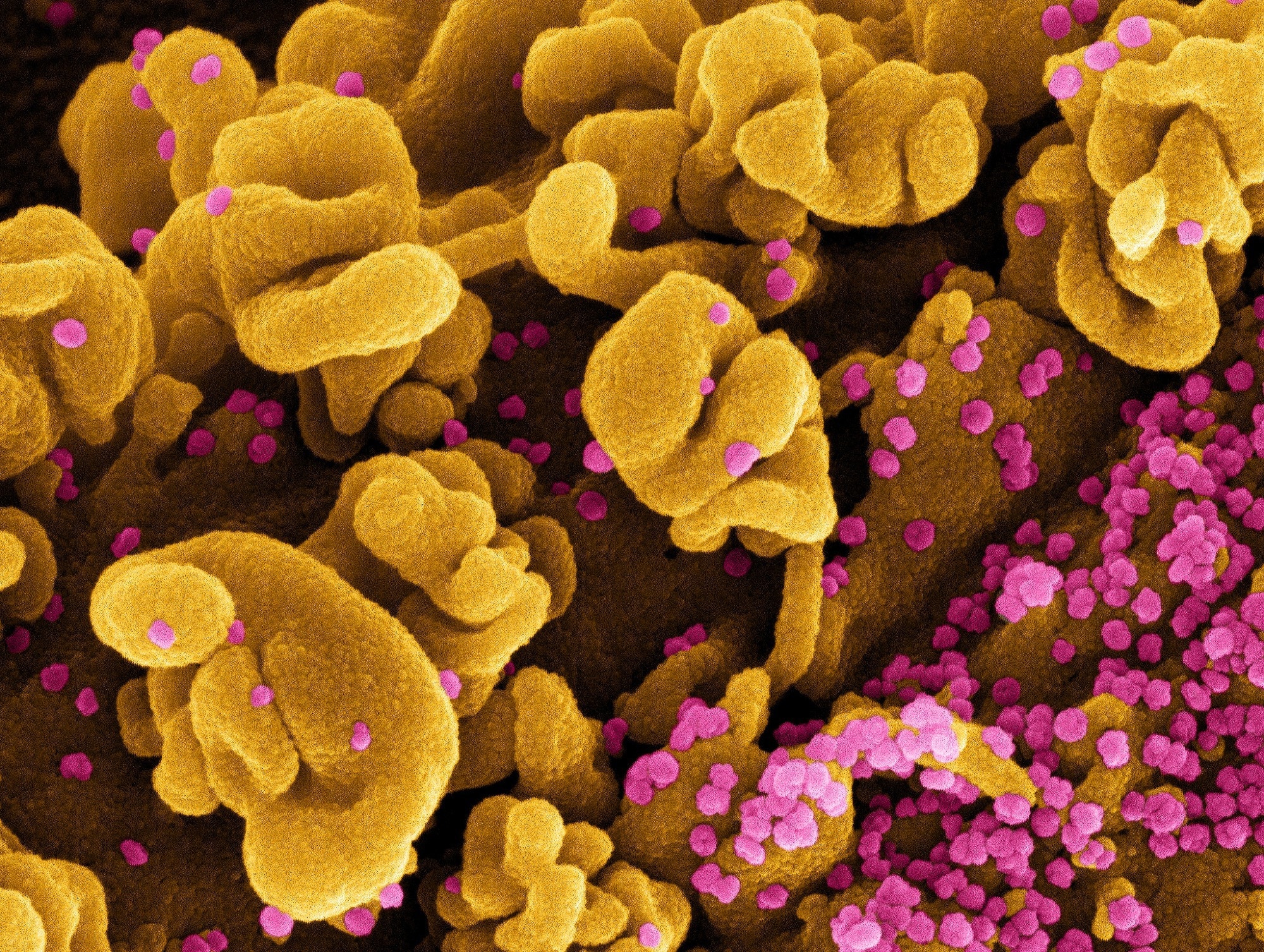
Исследование: микробиота кишечника и COVID-19: возможные последствия для тяжести заболевания. Изображение предоставлено: nobeastsofierce / Shutterstock.com
Введение
Предыдущие исследования подчеркивали важность кишечного микробиома в регуляции воспалительных процессов как на местном, так и на системном уровне. Из-за его широкой связи с другими органами и системами в организме микробиом также называют «вторым мозгом» тела.
Было показано, что риск дисбиоза кишечника увеличивается во время инфекции SARS-CoV-2, а также при пост-острых последствиях COVID (PASC), последний из которых более известен как «длительный COVID». В этих ситуациях сообщалось о повышенной концентрации условно-патогенных видов, в то время как количество «хороших» бактерий снижалось. Однако верно и обратное: у пациентов с меньшим количеством кишечных симптомов меньше шансов на клиническое ухудшение.
Дисбактериоз провоцирует воспаление
SARS-CoV-2 получает доступ к клетке-хозяину-мишени, связывая свой рецептор-связывающий домен (RBD) в субъединице вирусного спайкового белка S1 с рецептором ангиотензинпревращающего фермента 2 (ACE2).
Рецептор ACE2 также играет жизненно важную роль в ренин-ангиотензин-альдостероновой системе (РААС), которая регулирует кровяное давление. Следовательно, снижение активности ACE2 во время инфекции SARS-CoV-2 может повлиять на функцию РААС.
Цитокиновый шторм , характеризующийся чрезмерным выбросом цитокинов, часто возникает при тяжелом течении COVID-19. Это возникает после обнаружения инфицированных клеток клетками врожденного иммунитета, что впоследствии вызывает гипервоспалительный иммунный ответ. Цитокины высвобождают провоспалительные молекулы-мессенджеры, такие как интерлейкин-1 (ИЛ-1), ИЛ-6, ИЛ-8, ИЛ-12, фактор некроза опухоли α (ФНО-α) и интерферон γ (ИФН-γ) при высокой температуре. уровней в циркуляцию.
Затем цитокиновый шторм вызывает системную вазодилатацию и увеличивает сосудистую проницаемость, что приводит к тромботическим осложнениям, отеку легких и полиорганной недостаточности. Критические и летальные исходы более вероятны, если они возникают у людей с другими факторами риска сердечно-сосудистых заболеваний или тромбоза. Системное повреждение и полиорганная дисфункция характеризуют острый респираторный дистресс-синдром (ОРДС).
Дисбактериоз вызывает системные эффекты
Примерно у каждого пятого пациента с COVID-19 в какой-то момент во время инфекции развивается диарея с дискомфортом или болью в животе или без них. Вирусная РНК, по-видимому, сохраняется в слизистой оболочке кишечника и стуле ранее инфицированных пациентов в течение более одного месяца с момента появления симптомов. В дополнение к прямому повреждению клеток кишечника SARS-CoV-2, вероятно, вызывает повреждение кишечника через эту воспалительную среду.
Некоторые пациенты с COVID-19 с диареей демонстрируют более высокие уровни цитокинов в сыворотке, вероятно, из-за связывания вирусного белка с белками эпителиальных клеток, которые помогают формировать плотные контакты. Возникающее в результате нарушение эпителиального барьера кишечника нарушает внутриклеточный ионный баланс, вызывая колит и воспаление стенок кишечника. Кроме того, это может позволить кишечным бактериям попасть в системный кровоток, тем самым способствуя системному иммуноопосредованному воспалительному повреждению.
Высокая экспрессия ACE2 в эпителии кишечника является ключом к обеспечению стабильного и здорового состава и функции микробиома. И наоборот, когда экспрессия ACE2 снижается, потребление натрия и аминокислот также снижается, что увеличивает восприимчивость к воспалению кишечника.
Снижение экспрессии ACE2 в кишечном эпителии ослабляет мишень пути рапамицина (mTOR) у млекопитающих, тем самым изменяя экспрессию антимикробных пептидов (AMP) с усилением аутофагии. Вмешательство в эти взаимодействующие процессы ставит под угрозу выживаемость энтероцитов.
Ослабление кишечного барьера приводит к хронической дисфункции кишечника и изменению всасывания аминокислот, таких как фенилаланин, триптофан, глютамин и лейцин. Эти эффекты могут привести к воспалению, диарее и дисбактериозу.
Дисбактериоз увеличивает уязвимость к респираторным инфекциям и их клиническую тяжесть. Например, мыши с дисбиозом кишечника, вызванным антибиотиками, более восприимчивы к воспалению легких, вызванному гриппом.
Дисбактериоз увеличивает тяжесть COVID-19

Несколько предыдущих исследований показали, что COVID-19, вероятно, будет менее тяжелым при наличии повышенной численности семи классов бактерий, в частности Faecalibacterium prausnitzii и Alistipes onderdonkii . Оба этих вида микроорганизмов регулируют метаболизм триптофана и иммунный гомеостаз. Уровни Faecalibacterium prausnitzii часто низкие в западной диете, но высокие в средиземноморской диете.
Тяжелая форма COVID-19 также коррелирует с присутствием Coprobacillus , Clostridiumramosum , C. hathaway и Erysipelotrichaceae . Кроме того, присутствие Coprobacillus тесно связано с диареей и воспалением при заболевании раздраженного кишечника (ВЗК).
Примечательно, что несколько видов Bacteroides снижают экспрессию ACE2 в толстой кишке крыс и связаны с менее тяжелым течением COVID-19.
Бактериальные метаболиты, такие как короткоцепочечные жирные кислоты (КЦЖК), которые образуются в результате бактериальной ферментации пищевых волокон, также могут иметь отношение к гомеостазу. Бутират особенно важен, поскольку он поддерживает целостность эпителиального барьера кишечника, модулируя иммунные и воспалительные пути во всем организме.
SCFAs также действуют многими другими способами, чтобы уменьшить воспаление. Например, дисбактериоз кишечника снижает выработку SCFAs за счет сокращения соответствующих бактериальных таксонов, одновременно способствуя обилию условно-патогенных микроорганизмов. Эти микроорганизмы могут проникать через ослабленный барьер слизистой оболочки кишечника, впоследствии вызывая вторичную инфекцию у уже уязвимого человека и увеличивая риск тяжелых или смертельных исходов.
COVID-19 вызывает дисбактериоз
У пациентов с COVID-19 микробиом кишечника изменен с меньшим количеством комменсальных бактерий основных видов, таких как Bacteroides , полезные Lachnospiraceae и Bifidobacterium . Одновременно увеличивается количество условно-патогенных микроорганизмов, таких как Streptococcus , Rothia и некоторые виды Clostridia , такие как C. hathawayi .
Повышенные признаки воспаления, такие как С-реактивный белок (СРБ), лактатдегидрогеназа (ЛДГ), гамма-глутамилтрансфераза (ГГТ) и уровни циркулирующих ИЛ-6, ИЛ-10, ИФН-γ и ФНО-α, имеют также сообщалось. Эти изменения сохранялись даже через месяц после элиминации вируса.
Пробиотики снижают тяжесть течения COVID-19
Пробиотики, особенно те, которые содержат виды Bifidobacterium , сокращают время инфекций верхних дыхательных путей благодаря своему противовоспалительному действию, опосредованному их модуляцией кишечного микробиома. Таким образом, исследования показывают, что добавки с пробиотиками могут снизить тяжесть течения COVID-19.
Ранее пробиотики повышали уровень вирусспецифических иммуноглобулинов M (IgM) и IgG, не вызывая существенного изменения профиля фекальной микробиоты. Это указывает на прямое действие IgG на иммунитет, а не на изменение состава микробиома кишечника.
ACE и тяжесть COVID-19
В нескольких исследованиях было выявлено, что пациенты с ранее существовавшими заболеваниями легких, раком, твердыми трансплантатами, пожилым возрастом (70 лет и старше), ожирением, сердечно-сосудистыми заболеваниями и метаболическим синдромом имеют более высокий риск тяжелого и летального исхода COVID-19. Это может быть связано с изменениями в активности ACE2 с участием РААС. Например, пациенты с раком легких или диабетом экспрессируют ACE2 на более высоком исходном уровне.
Инфекция SARS-CoV-2 вызывает повышенную экспрессию ACE2 в легких и почках, особенно у пожилых пациентов и пациентов с хроническими заболеваниями легких, диабетом и гипертонией. Это может привести к чрезмерной активации оси АПФ-ангиотензин II-ангиотензин-1 рецептор.
Последствия этих действий включают повреждение и дисфункцию сосудов, воспаление и фиброз легких и сердечной мышцы, повреждение почек и резистентность к инсулину с усилением окислительного стресса.
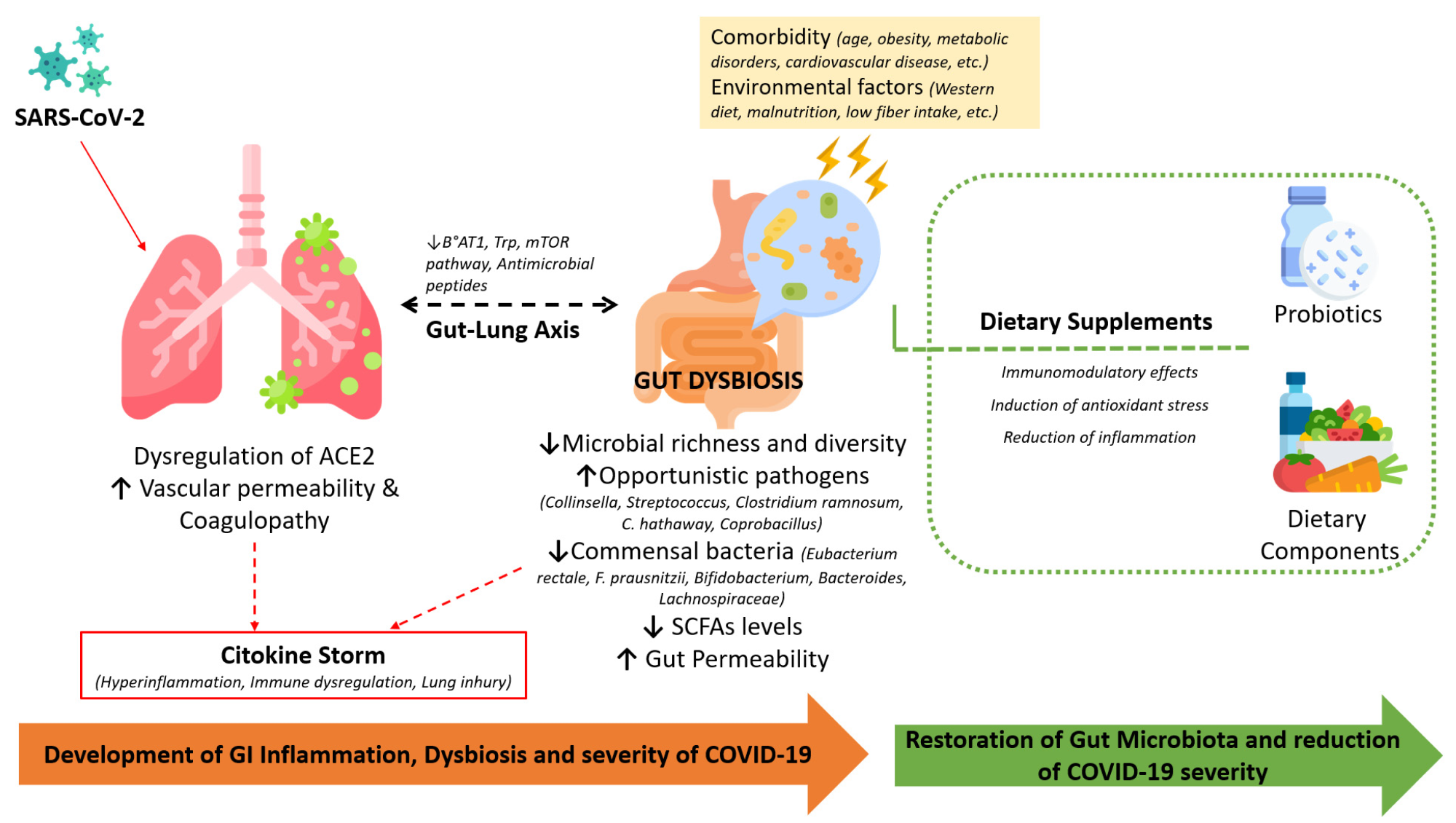
Участие вызванной инфекцией дисрегуляции ACE-2, сопутствующих заболеваний и изменений в микробиоте кишечника во время COVID-19, а также благотворное влияние пищевых добавок на восстановление микробиоты и иммунного гомеостаза.
Питание и COVID-19
У лиц с ожирением наблюдается хроническое слабовыраженное воспаление с высоким уровнем медиаторов воспаления, продуцируемых отложениями висцерального жира и врожденными иммунными клетками. Это повышает риск цитокинового шторма после вирусной инфекции, усугубляемый сопутствующим дисбиозом кишечника и давлением на легкие.
Страны Восточной Азии, многие из которых преимущественно потребляют рис, сообщили о гораздо более низких показателях смертности от COVID-19, чем страны остального мира, потребляющие пшеницу.
Витамин D модулирует функцию Т-клеток, впоследствии уменьшая медиаторы воспаления и увеличивая количество противовоспалительных молекул, таких как ИЛ-10, и его действие на функцию врожденного иммунитета. Добавки с витамином D могут снизить риск тяжелой инфекции и смерти, связанной с COVID-19.
Витамины C, E и A, а также такие металлы, как цинк и железо, являются мощными противовоспалительными и антиоксидантными соединениями, которые действуют различными путями. Поддержание омега-3 жирных кислот на адекватном уровне при сохранении их соотношения с омега-6 жирными кислотами на уровне 1:5, соответственно, является потенциально важной защитной мерой. В целом, растительная диета, обогащенная функциональными продуктами и добавками, может помочь защитить от респираторных инфекций.
Выводы
Состав микробиома кишечника в значительной степени определяет, как иммунная система реагирует на различные патогены, включая SARS-CoV-2. Кроме того, дисбактериоз можно считать фактором риска и результатом тяжелого течения COVID-19.
Понятно, что вмешательства, направленные на восстановление правильного состава микробиоты, важны для разработки более целостного подхода к лечению ряда заболеваний, включая COVID-19 …. стратегии, направленные на модификацию образа жизни и диеты, могут помочь положительно повлиять на микробиом кишечника и сыграть превентивную роль в вирусной инфекции SARS-CoV-2 ».
























Оставить Комментарий
Вы должны войти, чтобы оставить комментарий.